ZHAW-Forschende nutzen Algorithmen zur Optimierung von synthetisch wertvollen Enzymen
Enzyme gelten als Hoffnungsträger der chemischen Industrie auf dem Weg zu mehr Nachhaltigkeit. Ein Forschungsteam der ZHAW optimiert solche Enzyme für den Einsatz in der Industrie. Kürzlich wurde ein Forschungsprojekt des Instituts für Chemie und Biotechnologie im renommierten Fachmagazin Nature Communications publiziert. Dabei geht es um die erfolgreiche algorithmengestützte Optimierung eines Enzyms, das kleine Moleküle halogenieren kann.
Enzyme sind Proteine, die für das Ablaufen vieler lebenswichtiger Prozesse in Lebewesen sorgen. Als natürliche Biokatalysatoren können sie chemische Prozesse «grüner» gestalten. Dies macht sich die Industrie zunutze, um durch den Einsatz von Enzymen auf giftige Chemikalien, seltene Metalle und extreme Reaktionstemperaturen verzichten zu können.
Enzyme müssen für den industriellen Einsatz optimiert werden
Enzyme sind über viele Milliarden Jahre durch die Evolution für ihre Funktion optimiert worden. In der Industrie haben Enzyme aber andere Aufgaben zu erfüllen als in der Natur. Um die natürlichen «Alleskönner» auch in der industriellen Produktion einsetzen zu können, müssen sie für ihre neuen Aufgaben optimiert werden. Das geschieht mittels «gerichteter Evolution», einem Verfahren, das im Jahr 2018 mit dem Nobelpreis für Chemie (an die US-Forscherin Frances Arnold) honoriert wurde.
ZHAW-Forschende entwickeln massgeschneidertes Enzym zur Halogenierung von Naturstoffen
Das Forschungsteam von Rebecca Buller am ZHAW-Institut für Chemie und Biotechnologie in Wädenswil nutzt dieses Verfahren, um Enzyme für die industrielle Verwendung zu optimieren. Im Forschungsprojekt, das im renommierten Fachjournal Nature Communications publiziert wurde, haben die Chemikerinnen und Chemiker das Wildtyp-Enzym «Wel05*» erstmals so verändert, dass es einen industriell relevanten, für das Enzym jedoch fremden Naturstoff halogeniert. Halogenierende Enzyme sind interessant für die chemische und pharmazeutische Industrie. Als Biokatalysatoren können sie sehr spezifisch beispielsweise Chlor oder Brom in eine chemische Verbindung einfügen, mit dem Ziel, deren Bioaktivität zu verändern. Beim industriell relevanten Naturstoff, den das an der ZHAW massgeschneiderte Enzym «Wel05*» erstmals halogeniert, handelt es sich um ein Fungizid, also einen pilzabtötenden Wirkstoff. Das Enzym «Wel05*» optimierten die Forschenden weiter, bis sie eine Halogenase-Variante fanden, welche die 300fache Menge des Fungizids umsetzen konnte und dies mit 90facher Geschwindigkeit. Sie haben die Produktivität der Halogenase also massiv gesteigert und auf diese Weise selektivere Derivate des potenten Fungizids entwickelt.
Kombination von Enzymbibliotheken und maschinellem Lernen eingesetzt
Gelungen ist dies dem Forschungsteam um Rebecca Buller mit einer richtungsweisenden Kombination aus Enzymbibliotheken und maschinellem Lernen. «Mittels Enzym Engineerings können wir Aminosäuren in einem Enzym austauschen und so seine Aktivität verändern. Dieses Verfahren eröffnet aber so viele Aminosäurekombinationen, dass wir nicht alle experimentell durchspielen können. Darum produzieren und testen wir nur einen Bruchteil der möglichen Enzymvarianten im Labor – und nutzen Algorithmen, um uns auf Basis dieser Daten noch bessere Kombinationen vorherzusagen zu lassen», erklärt Rebecca Buller das Potential der Methode.
Halogenasen eröffnen neue Synthesewege in der Medizinalchemie
Die von den Forschenden entwickelten Halogenasen eröffnen bereits jetzt neue Synthesewege in der Medizinalchemie. Sie können im kleinen Massstab eingesetzt werden, um im Labor neue Wirkstoffe zu entwickeln, so wie die in der Publikation vorgestellten Fungizide. In einem nächsten Schritt werden die Forschenden «WelO5*» auch für den grösseren Massstab optimieren und ihre Methode auf andere Enzymklassen anwenden. So könnten die Halogenasen der ZHAW in Zukunft eine nachhaltige Alternative in der chemischen und pharmazeutischen Produktion werden.
Downloads
- Medienmitteilung «ZHAW-Forschende nutzen Algorithmen zur Optimierung von synthetisch wertvollen Enzymen»(PDF 138,2 KB)
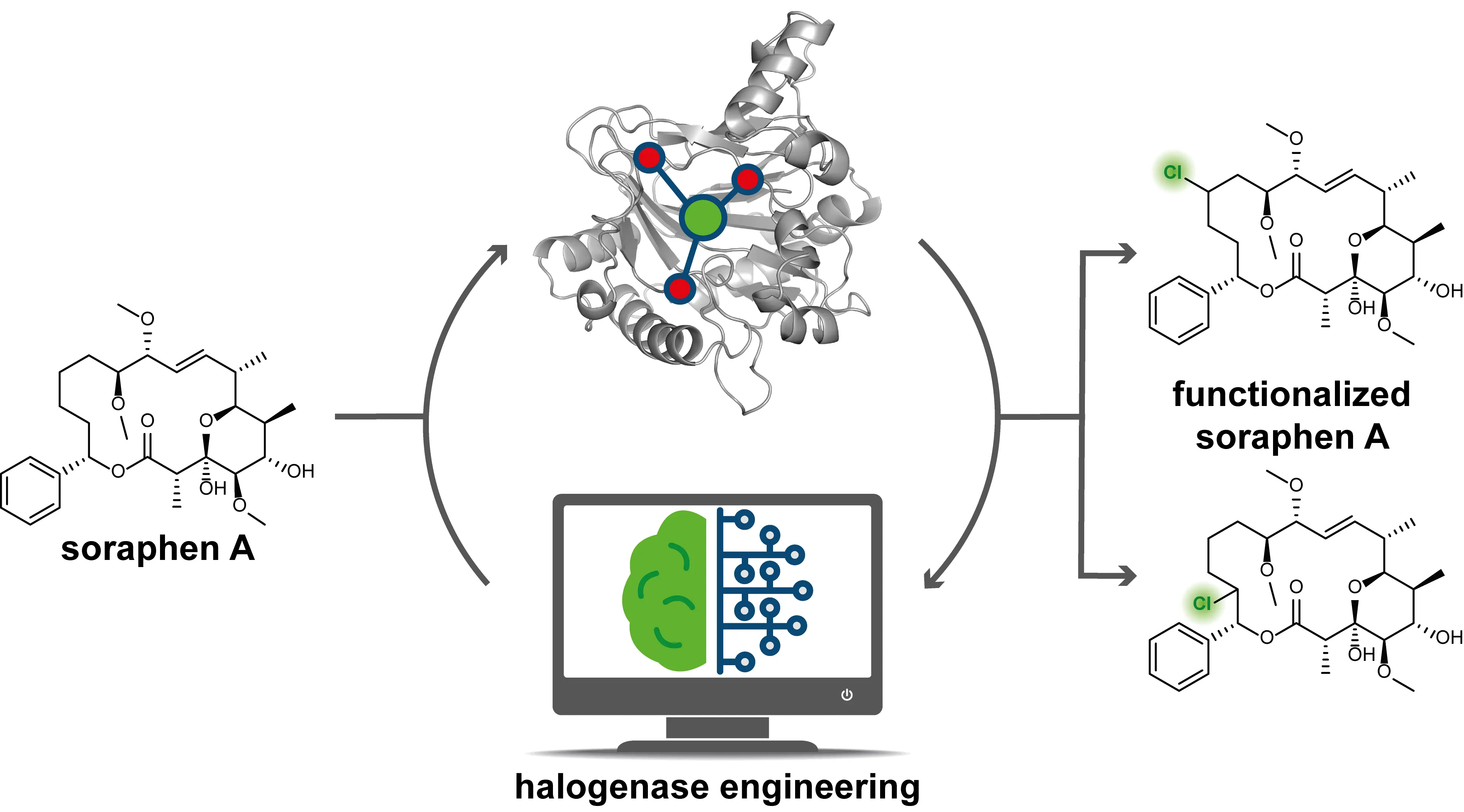
- Bild 1: Soraphen A, ein potentes Fungizid, wird mittels algorithmen-optimierter Enzyme passgenau derivatisiert. Die funktionalisierten Derivate des Fungizids zeichnen sich durch ihre geänderte Bioaktivität aus. / Grafik © ZHAW/Johannes Büchler(TIFF 2,7 MB)
- Bild 2: Mit dem Einsatz einer massgeschneiderten Automatisierungsplattform und maschinellem Lernen optimiert Rebecca Buller vom ZHAW-Kompetenzzentrum für Biokatalyse Enzyme für den Einsatz in der Industrie. / Foto © ZHAW/Brüderli
Fachkontakt
- Rebecca Buller, Leiterin Fachstelle Biokatalyse, Umwelt- und Prozesstechnologie, Institut für Chemie und Biotechnologie, ZHAW-Departement Life Sciences und Facility Management, Wädenswil. 058 934 54 93, rebecca.buller@zhaw.ch
- Fachstelle Biokatalyse, Umwelt- und Prozesstechnologie: www.zhaw.ch/icbt/biokatalyse-und-prozesstechnologie/
Medienstelle ZHAW, Wädenswil
- Cornelia Sidler, Media Relations ZHAW-Departement Life Sciences und Facility Management, Wädenswil. 058 934 53 66, cornelia.sidler@zhaw.ch
Quelle/Publikation
- Büchler, J. et al. Algorithm-aided engineering of aliphatic halogenase WelO5* for the asymmetric late-stage functionalization of soraphens. Nat. Commun. 13, 371 (Januar 2022): https://www.nature.com/articles/s41467-022-27999-1